Aufgabe 3 – Brennstoffzelle und Meerwasser als Wasserstoffquelle
Brennstoffzellen werden mittlerweile in vielen Technikbereichen eingesetzt. Eine kostengünstige und nachhaltige Herstellung des dafür in großen Mengen benötigten Wasserstoff-Gases stellt die Forschung jedoch vor Probleme. Einen Ansatz zur Lösung liefert möglicherweise die Herstellung von Wasserstoff aus Meerwasser.
Beschreibe den Aufbau der in Material 1 abgebildeten alkalischen Brennstoffzelle.
Erläutere an den gegebenen Reaktionsgleichungen das Donator-Akzeptor-Prinzip (M 1).
Berechne die zu erwartende Zellspannung der alkalischen Brennstoffzelle unter Standardbedingungen (M 1).
Erkläre unter Verwendung der Nernst-Gleichung beider Halbzellen, dass der pH-Wert keinen Einfluss auf die Zellspannung dieser Brennstoffzelle hat (M 1, M 2).
Werte die Beobachtungen des Modellexperiments unter Einbeziehung von Berechnungen aus (M 3, M 4).
Formuliere die Reaktionsgleichungen für die an der Anode und Kathode ablaufenden Reaktionen (M 4).
Erkläre die Bedeutung der Überspannung für das Modellexperiment (M 3, M 4).
Begründe, dass das Modellexperiment nur eingeschränkt auf die Herstellung von Wasserstoff aus Meerwasser übertragbar ist (M 3).
Beurteile anhand von drei Argumenten, ob der Betrieb einer großtechnischen Anlage zur Herstellung von Wasserstoff auf offener See im Hinblick auf die dafür benötigten und zur Verfügung stehenden Ressourcen sinnvoll ist (M 5).
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Schematische Darstellung einer alkalischen Brennstoffzelle
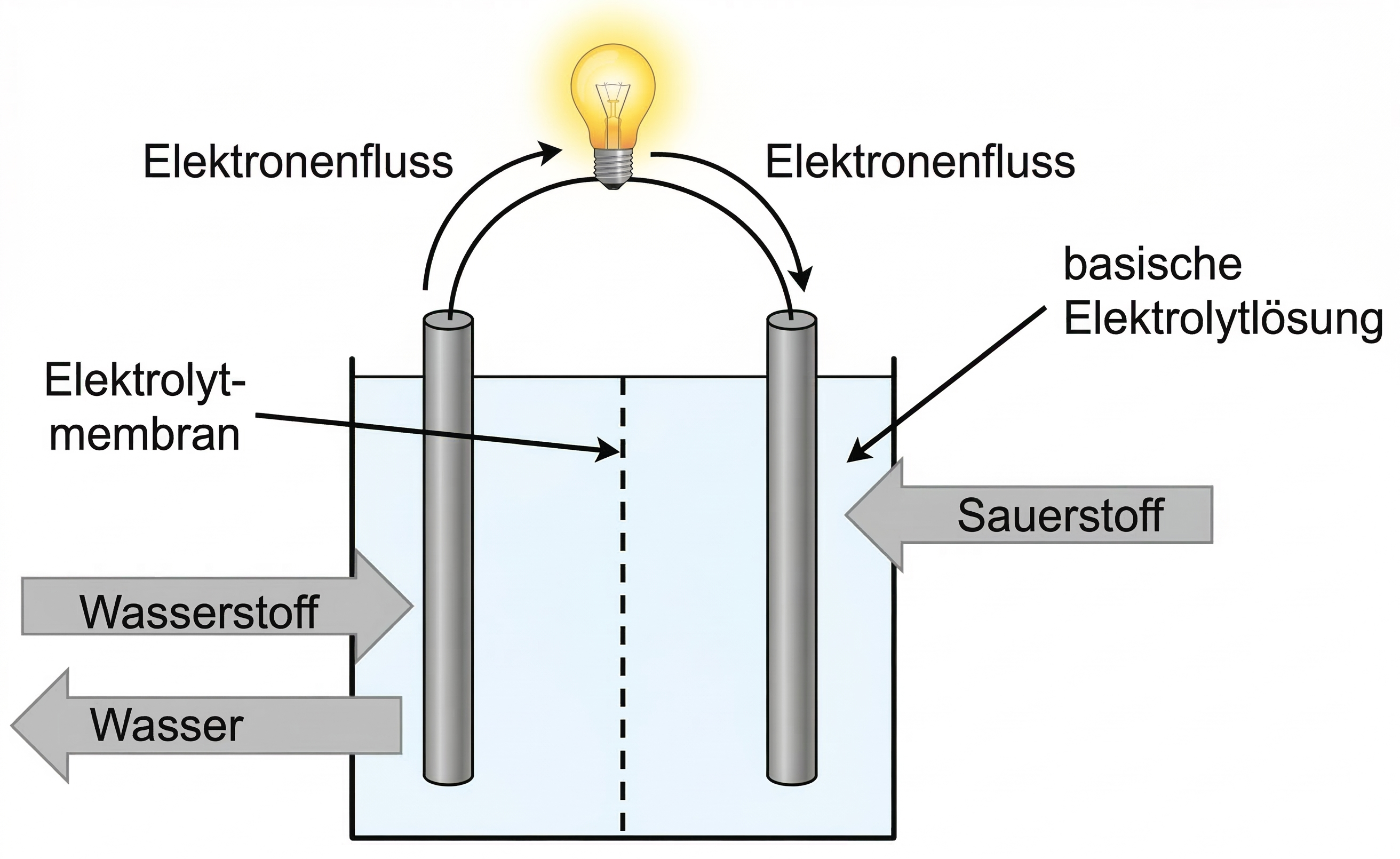
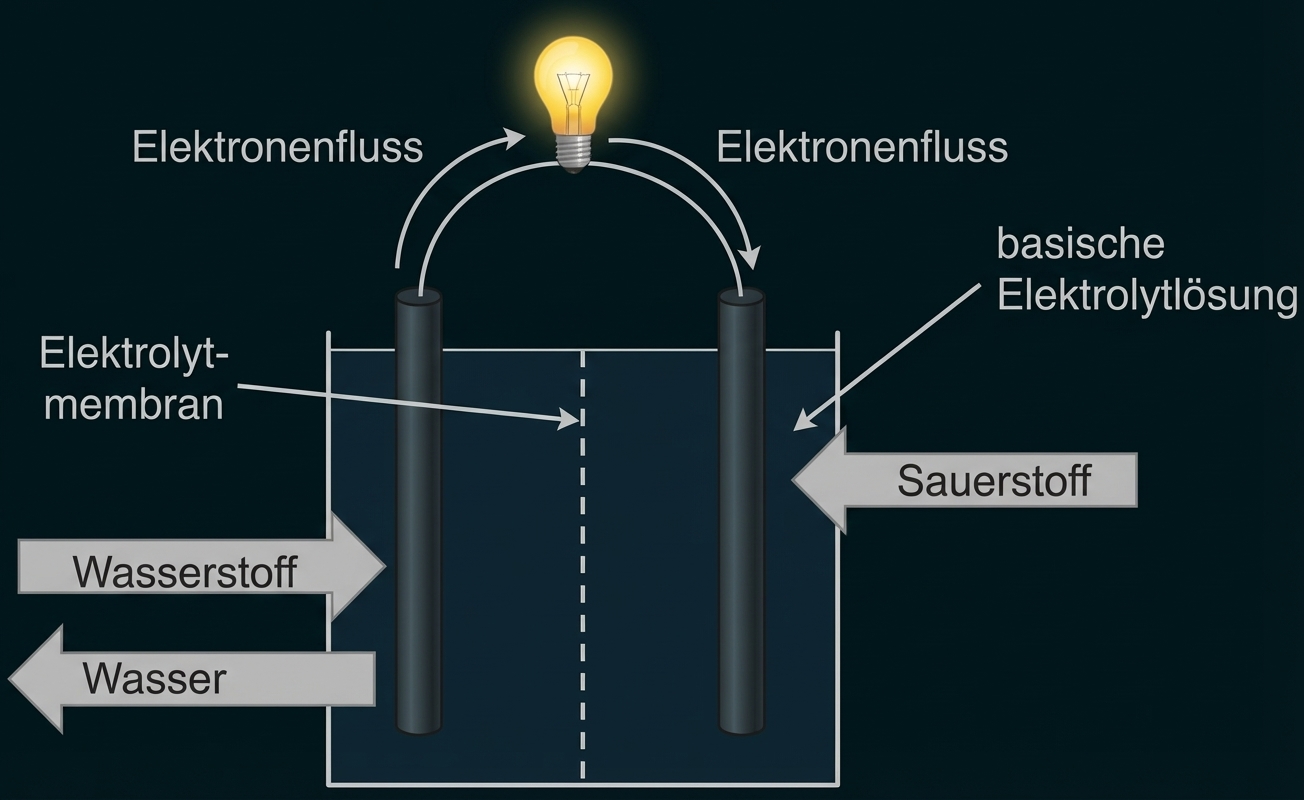
Abb. 1: Schematische Darstellung einer alkalischen Brennstoffzelle
Reaktionen in der alkalischen Brennstoffzelle:
|
• Anodenreaktion: |
|
|
• Kathodenreaktion: |
|
|
• Gesamtreaktion: |
|
-
Anodenreaktion:
-
Kathodenreaktion:
-
Gesamtreaktion:
Material 2: Nernst-Gleichung und Stoffmengenkonzentrationen in den Halbzellen einer alkalischen Brennstoffzelle
Nernst-Gleichung:
Für die Anoden-Halbzelle gilt:
Für die Kathoden-Halbzelle gilt:
Material 3: Modellexperiment zur Herstellung von Wasserstoff
Versuchsaufbau und Durchführung:
Zur Herstellung von Wasserstoff wird ein U-Rohr mit einer Elektrolytmembran mit einer wässrigen Natriumchlorid-Lösung und einigen Tropfen Phenolphthalein-Lösung befüllt. An jeder Seite des U-Rohres taucht eine Graphitelektrode in die Lösung ein. Beide Elektroden sind durch eine Gleichspannungsquelle miteinander verbunden. Um die Reaktion zu starten, wird eine Spannung von Volt angelegt.
Beobachtungen:
-
Sobald die Gleichspannungsquelle angeschaltet wird, bilden sich an beiden Elektroden Bläschen.
-
In einer der beiden Halbzellen wird die Lösung pink.
[1]
Material 4: Informationen zu den bei dem Modellexperiment relevanten Reaktionen
Tab. 1: Standardpotentiale relevanter Redoxpaare im Modellexperiment und Überspannungen der zugehörigen Elektrodenreaktionen an der Graphitelektrode
|
Redoxpaar |
|
(an Graphitelektroden; Stromdichte: |
|
|
Anode |
|
|
|
|
|
|
|
|
|
Kathode |
|
|
|
|
|
|
|
[2], [3]
Material 5: Informationen zur Herstellung von Wasserstoff aus Wasser
Wasserstoff kann mithilfe einer Elektrolyse aus Wasser hergestellt werden. Für ein Kilogramm Wasserstoff werden durchschnittlich Kilowattstunden Strom und neun Liter Wasser benötigt. Der erzeugte Wasserstoff wird per LKW, Bahn, Schiff oder Pipeline zum Verbraucher transportiert.
[4]
Quellen (ggf. verändert):
[1] Elektrolyse einer Natriumchlorid-Lösung (o. D.). http://www.unterrichtsmaterialien-chemie.uni-goettingen.de/material/9-10/V9-268.pdf (Zugriff am: 16.09.2024)
[2] Elektrolysen (o. D.). http://www.bhbrand.de/downloads/elektrolysen.pdf (Zugriff am: 03.01.2025)
[3] Überspannung (Elektrochemie) (o. D.) https://www.chemie.de/lexikon/Überspannung_%28Elektrochemie%29.html (Zugriff am: 03.01.2025)
[4] Wasserstoff-FAQs (o.D.). H2.B, Zentrum Wasserstoff, Bayern. https://h2.bayern/infothek/faqs/#:~:text=Für%20die%20Herstellung%20von%20einem,werden%209%20Liter%20Wasser%20benötigt. (Zugriff am: 16.09.2024)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Beschreibung des Aufbaus einer alkalischen Brennstoffzelle
-
Eine alkalische Brennstoffzelle ist mit einer basischen Elektrolytlösung gefüllt.
-
Eine Elektrode wird mit Wasserstoff und die andere mit Sauerstoff umspült.
-
Eine Elektrolytmembran trennt den Kathoden- von dem Anodenraum.
-
Beide Elektroden sind über einen Verbraucher leitend verbunden.
Erläuterung des Donator-Akzeptor-Prinzips
-
Je ein Wasserstoff-Atom im Wasserstoff-Molekül gibt ein Elektron ab (Elektronendonator).
-
Je ein Sauerstoff-Atom im Sauerstoff-Molekül nimmt zwei Elektronen auf (Elektronenakzeptor).
-
Elektronenübergang von Wasserstoff-Atomen zu Sauerstoff-Atomen aus den Molekülen
Berechnung der Zellspannung unter Standardbedingungen
Berechnung und Erklärung der pH-Unabhängigkeit
Die Zellspannung der alkalischen Brennstoffzelle ist unabhängig von der Konzentration der Hydroxid-Ionen. Somit ist sie auch unabhängig vom pH-Wert.
Auswertung des Experiments
-
Es handelt sich um eine Elektrolyse.
-
An der Bläschenbildung erkennt man die Entstehung von Gasen.
-
Aus den vorhandenen Edukten können Sauerstoff, Wasserstoff oder Chlor entstehen.
-
Die Pinkfärbung der Phenolphthalein-Lösung zeigt die Entstehung einer basischen Lösung.
-
An der mit dem Pluspol verbundenen Elektrode (Anode) findet die Oxidation statt.
-
An der mit dem Minuspol verbundenen Elektrode (Kathode) findet die Reduktion statt.
Aus den gegebenen Werten ergeben sich:
Die minimale Zellspannung errechnet sich mit:
Damit entstehen bei dem Experiment die Gase Chlor und Wasserstoff.
Formulieren der Reaktionsgleichungen
Erklärung der Bedeutung der Überspannung
-
Die elektrochemische Überspannung ist die reale Abweichung von berechneten Werten.
-
Somit ist das die Spannung, die man bei einer Elektrolyse zusätzlich zur Zellspannung anlegen muss, damit diese Elektrolyse ablaufen kann.
-
Die Gase weisen hohe Überspannungswerte an Graphitelektroden auf.
-
Im Modellexperiment muss daher eine Spannung von mindestens
Volt angelegt werden.
Begründung der eingeschränkten Übertragbarkeit
-
Das Meerwasser wird vereinfacht durch die Natriumchloridlösung dargestellt.
-
Ein möglicher Einfluss von anderen im Meerwasser enthaltenen Ionen oder von Verunreinigungen des Meerwassers wird nicht berücksichtigt.
Beurteilung einer Anlage auf offener See
-
Auf dem Meer ist der Zugang zu Energie aus Sonnenlicht und Wind vorhanden, die vor Ort nachhaltig zu elektrischer Energie umgewandelt werden kann.
-
Wasser als Edukt ist in großer Menge vorhanden und müsste nicht zur Anlage transportiert werden.
-
Die Transportwege für den hergestellten Wasserstoff zu den Verbrauchern sind ggf. länger und aufwendiger (Pipelines oder Schiffe sind notwendig).