A2 – Textilfärbung
Bei der Herstellung von gefärbten Textilien entstehen erhebliche Mengen an Abwasser. Diese können bei nicht fachgerechter Entsorgung zu Umwelt- und Gesundheitsschäden führen.
Beschreibe das Prinzip der Küpenfärbung am Beispiel von Indigo. Erkläre das Vorgehen beim Aufbringen des Farbstoffs und dessen Haftung an der Kleidungsfaser unter Verwendung von Reaktionsgleichungen. (M 1)
Interpretiere die Absorptionsspektren von Indigo und Leukoindigo (Abb. 3). Beurteile, ob sich die beiden MO-Schemata (Abb. 4) mit den Absorptionsspektren decken. (M 1)
Werte die Ergebnisse der fotometrischen Eichreihe von Säurerot aus (Tab. 2). Bestimme den molaren Extinktionskoeffizienten von Säurerot. (M 2)
Leite den Typ der Polyreaktion sowie die für die Synthese des angegebenen Aramids (Abb. 6) notwendigen Monomere ab. Vergleiche den Molekülbau und die thermischen Eigenschaften ausgehend vom Struktur-Eigenschafts-Prinzip der beiden Kunststoffe. (M 2)
Bewerte die beiden Verfahren zur Entfernung von Säurerot sowie die ungefilterte Einleitung von Färbereiabwässern in Flüsse unter dem Aspekt der Nachhaltigkeit. (M 2)
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Material 1: Indigo
Indigo ist eines der ältesten bekannten Pigmente und wird häufig zum Färben von Jeans eingesetzt. Das Färbeverfahren bei Indigo (Abb. 1) ist eine sogenannte Küpenfärbung, bei der in basischer Lösung Natriumdithionit zu Schwefeldioxid reagiert. Dabei bildet sich Leukoindigo (Abb. 2).
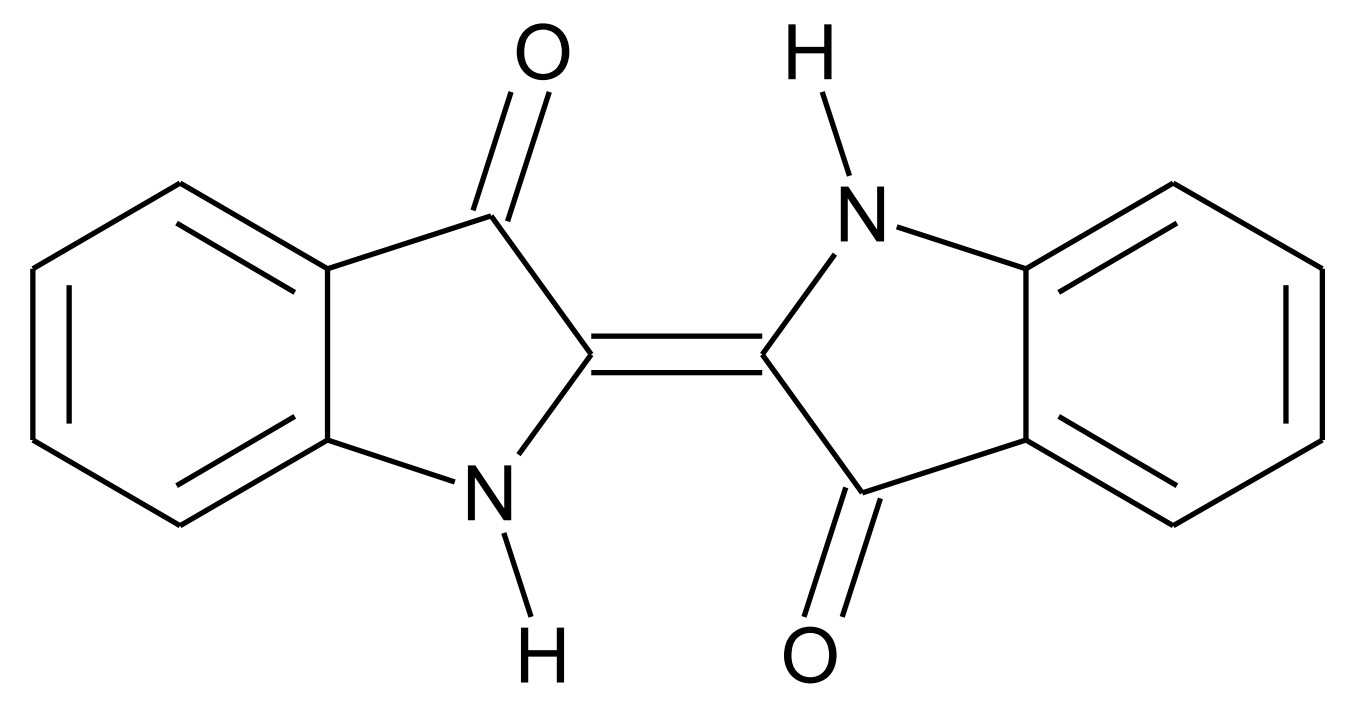
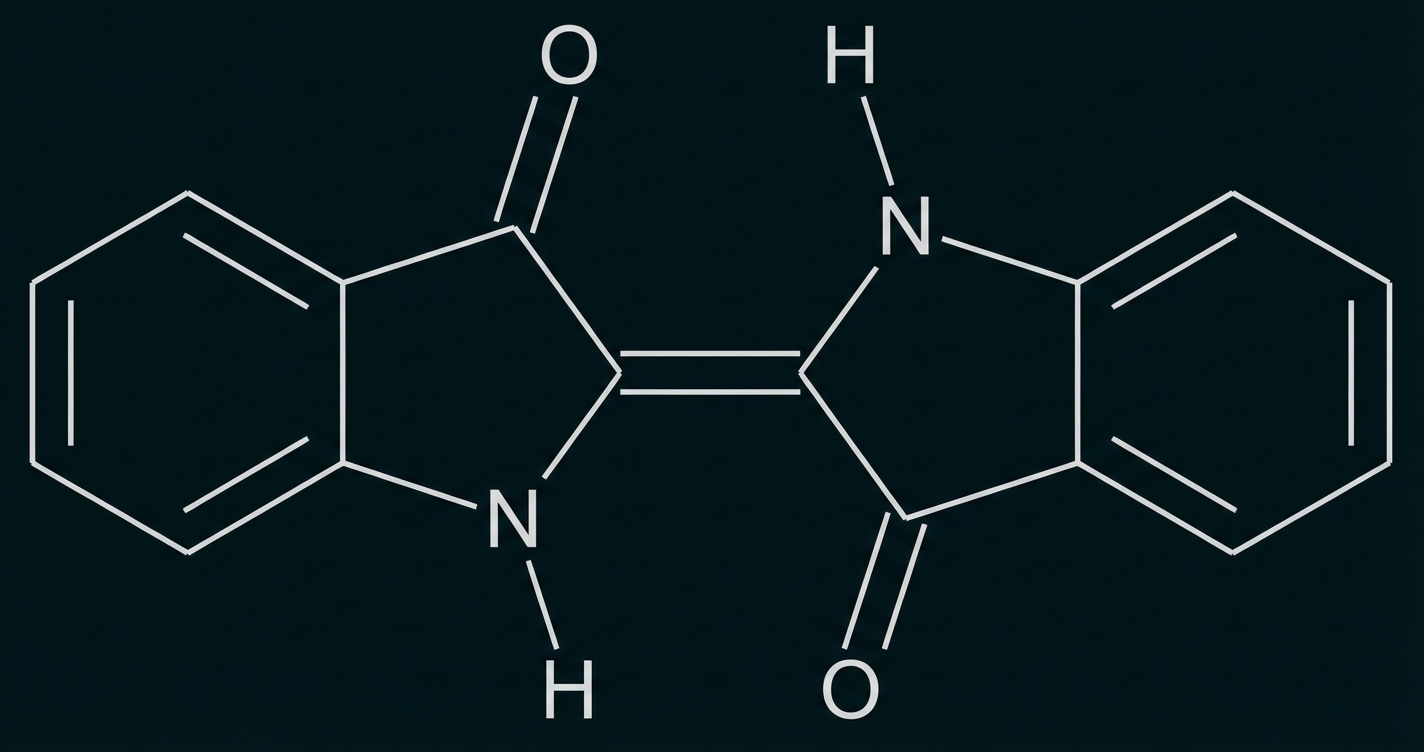
Abb. 1: Strukturformel von Indigo
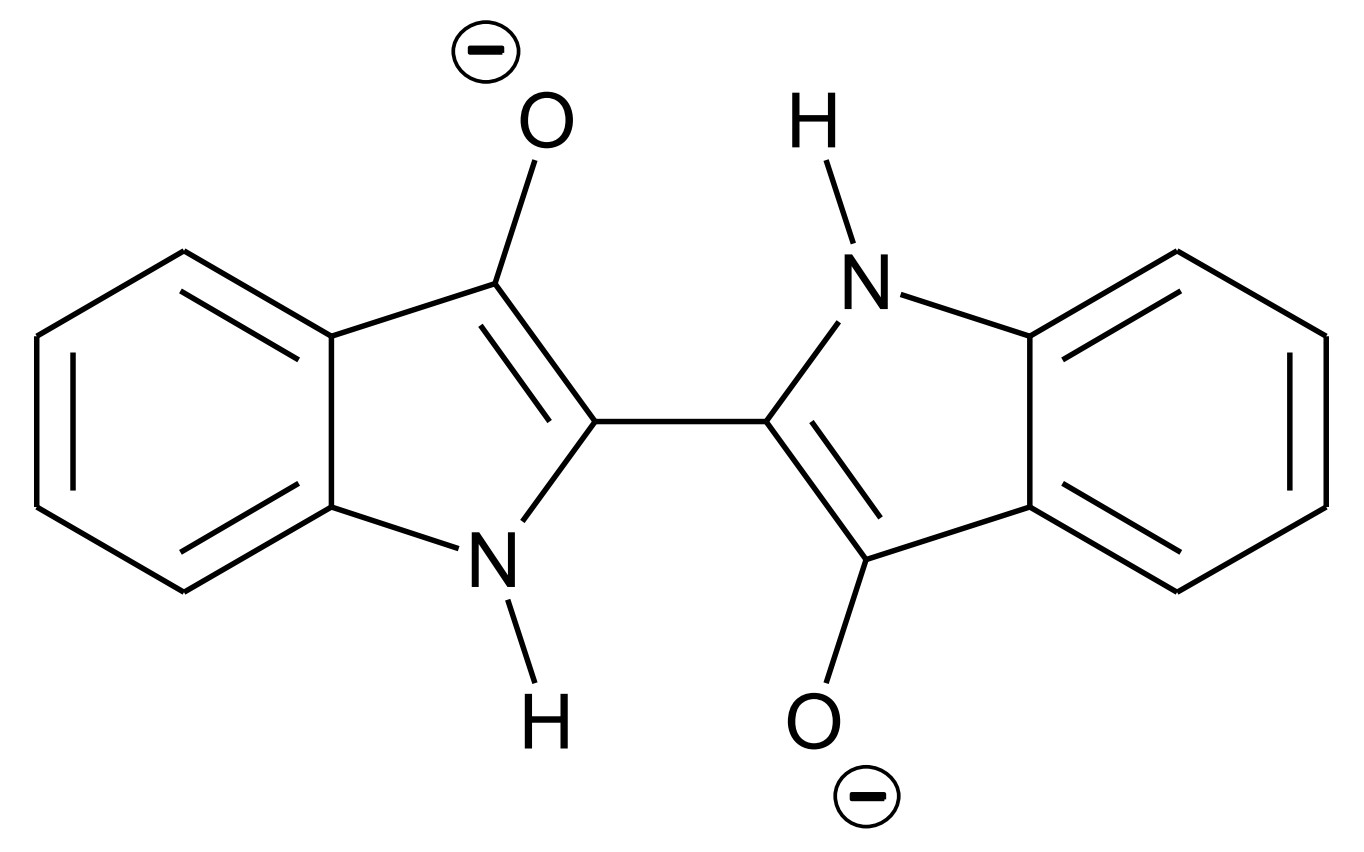
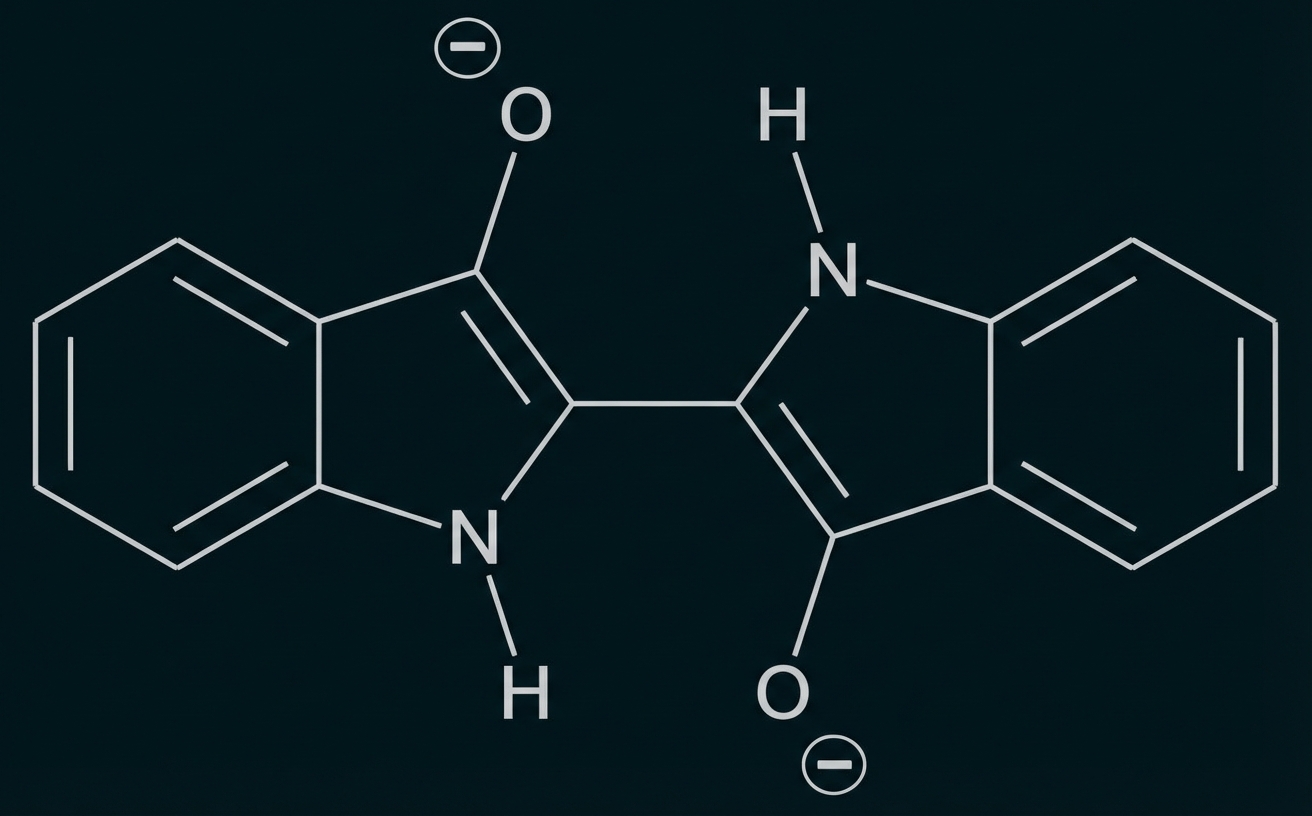
Abb. 2: Strukturformel von Leukoindigo
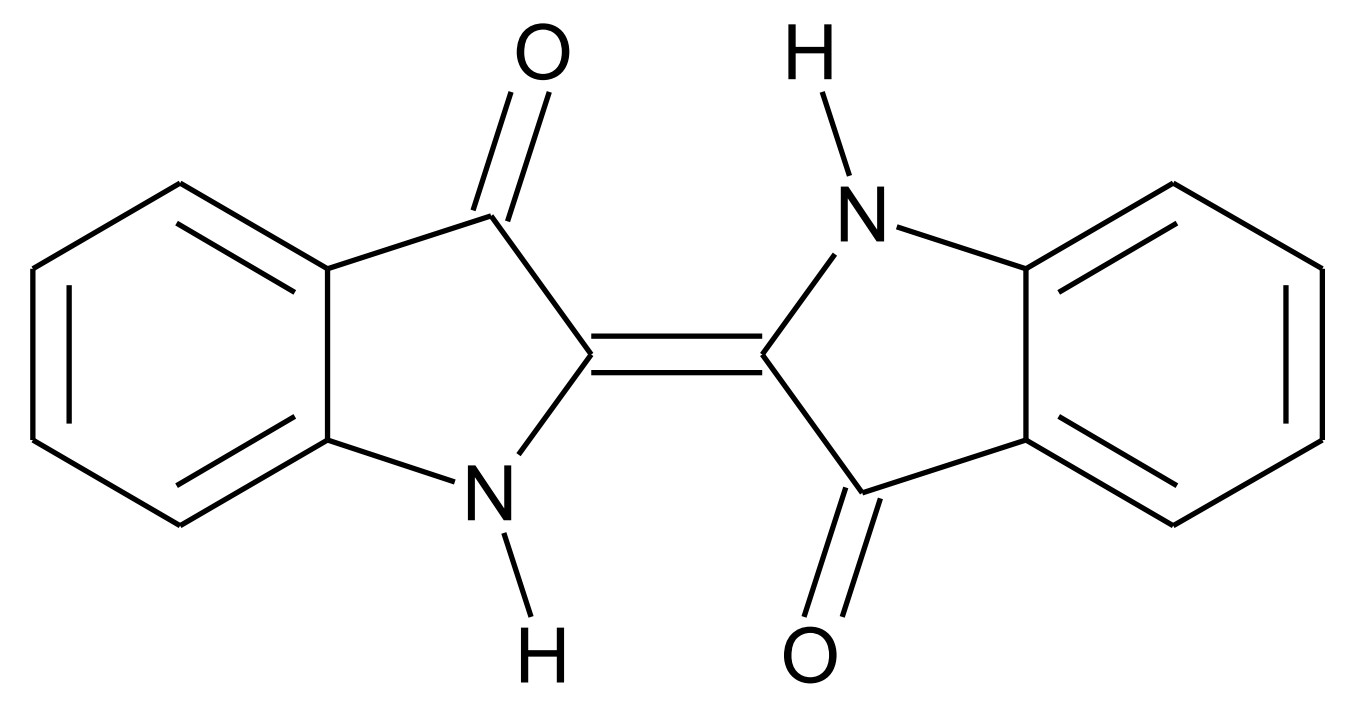
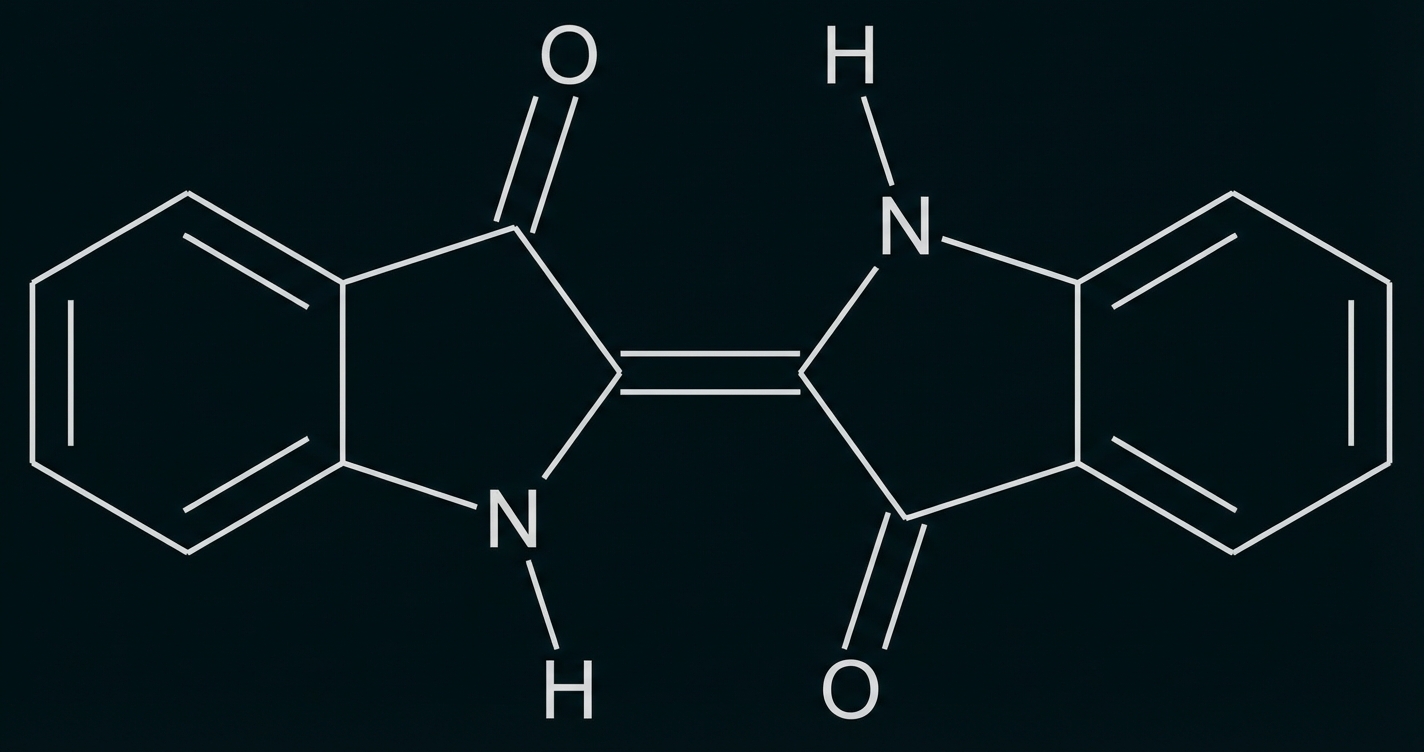
Abb. 1: Strukturformel von Indigo
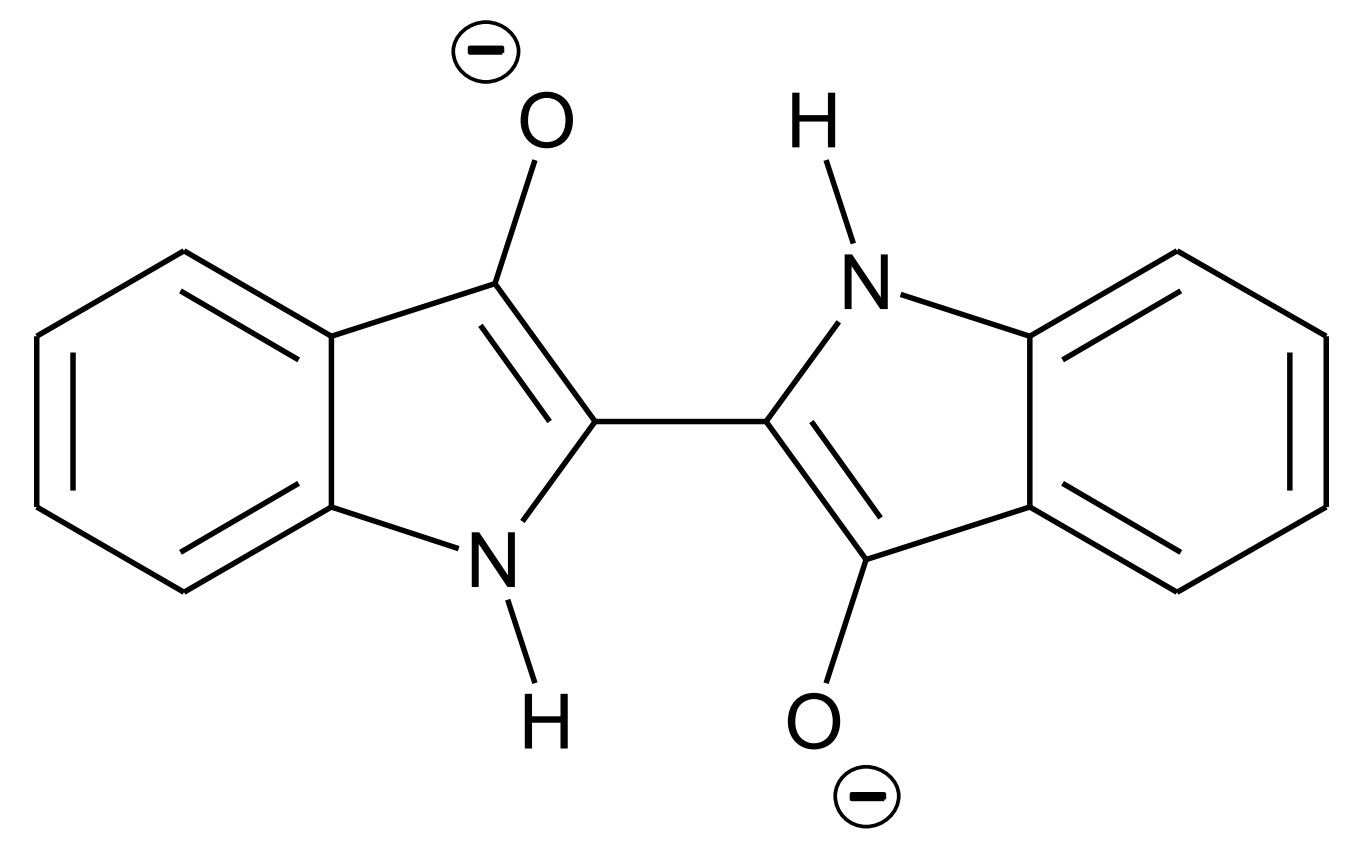
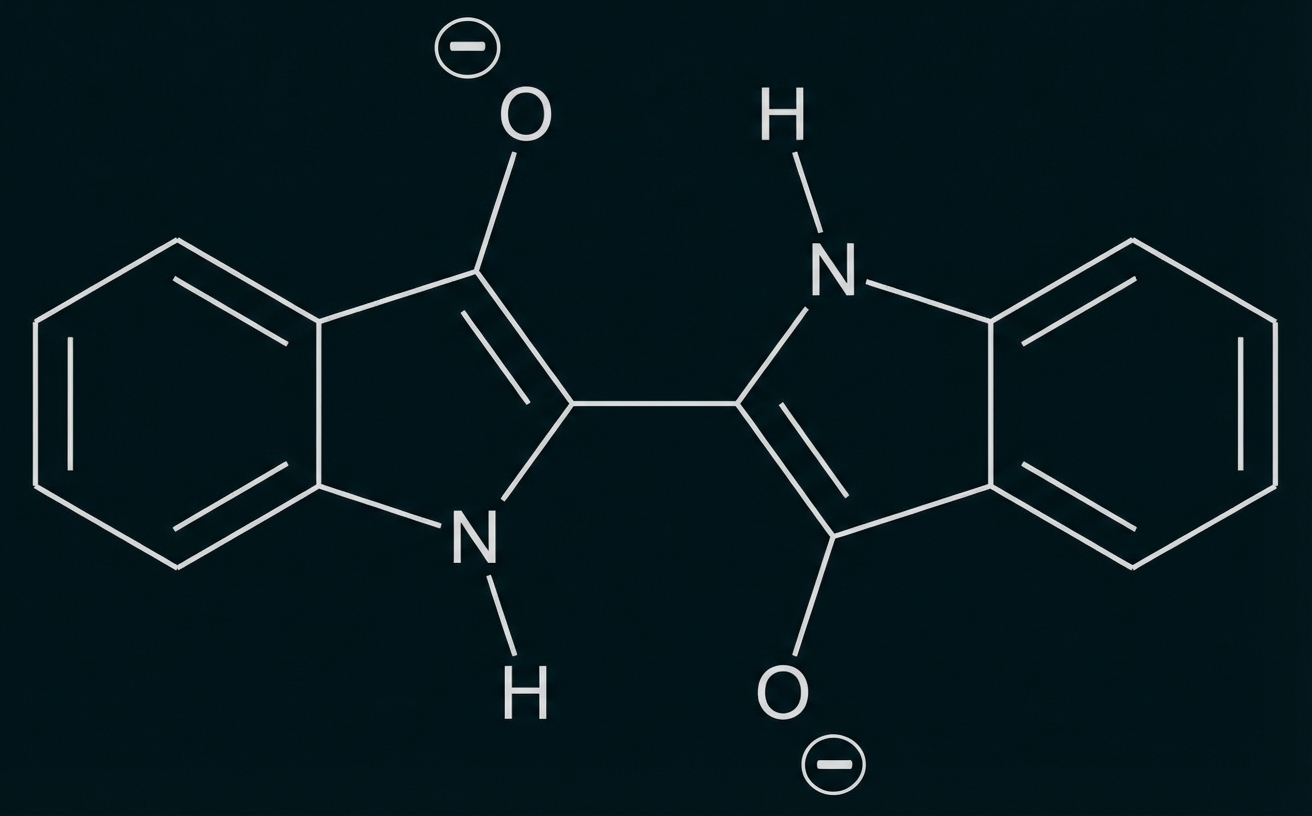
Abb. 2: Strukturformel von Leukoindigo
Um Absorptionsspektren von Farbstoffen erstellen zu können, müssen Stoffe in gelöster Form vorliegen. Indigo löst sich nur schlecht in Wasser, aber gut in Dimethylformamid. Dieses Lösemittel verschiebt das Absorptionsspektrum (Abb. 3) im Vergleich zu Wasser um einige Nanometer hin zu größeren Wellenlängen.
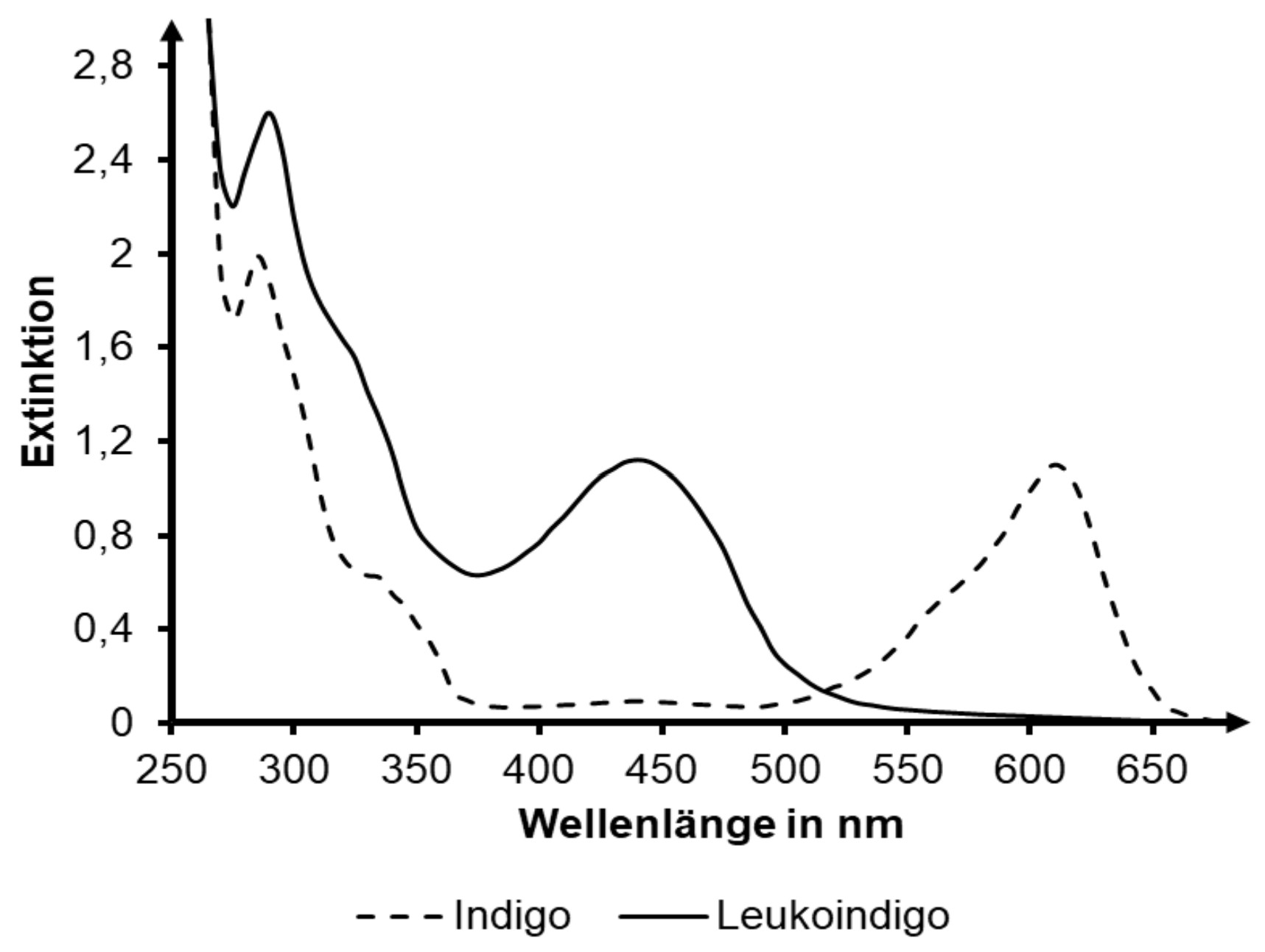
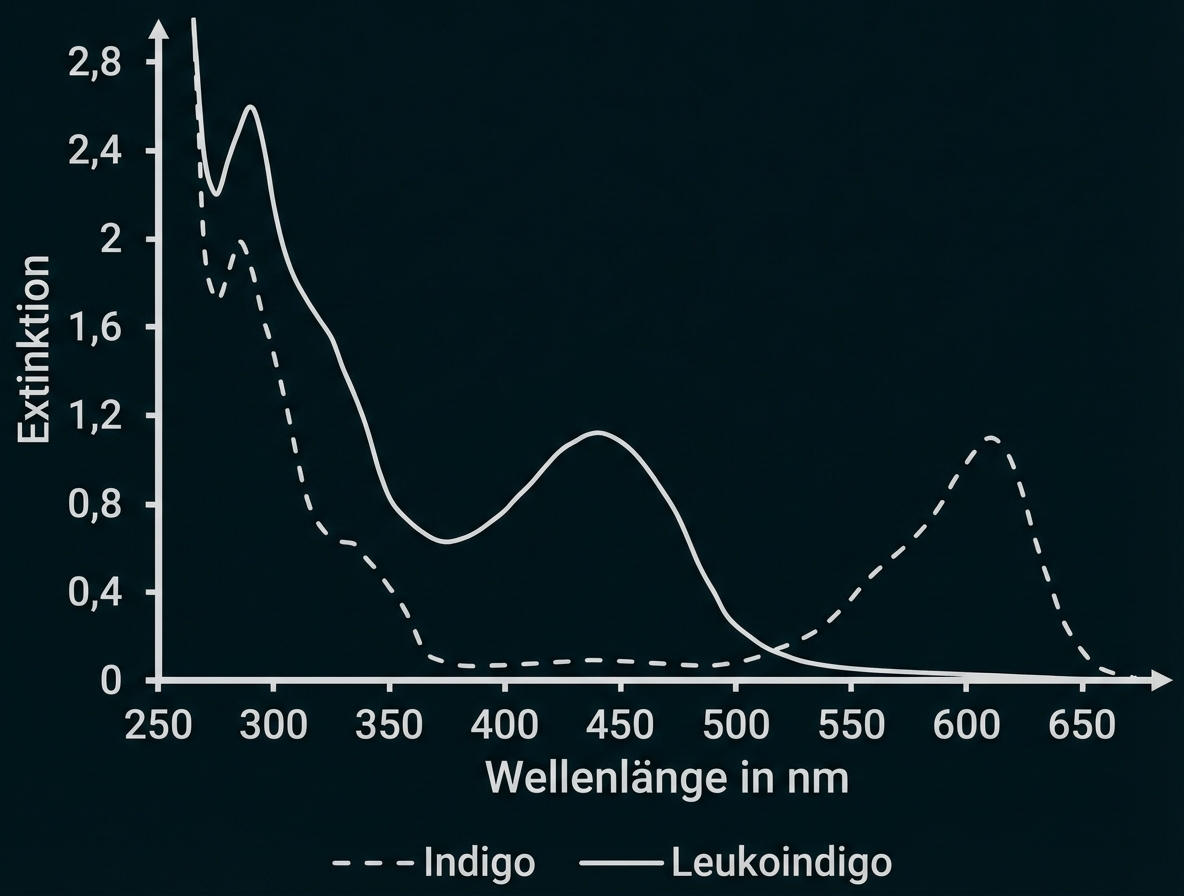
Abb. 3: Absorptionsspektren von Indigo und Leukoindigo in Dimethylformamid1
Zur Erklärung der Farbunterschiede von Indigo und Leukoindigo können folgende Molekülorbital-Schemata (Abb. 4) herangezogen werden.
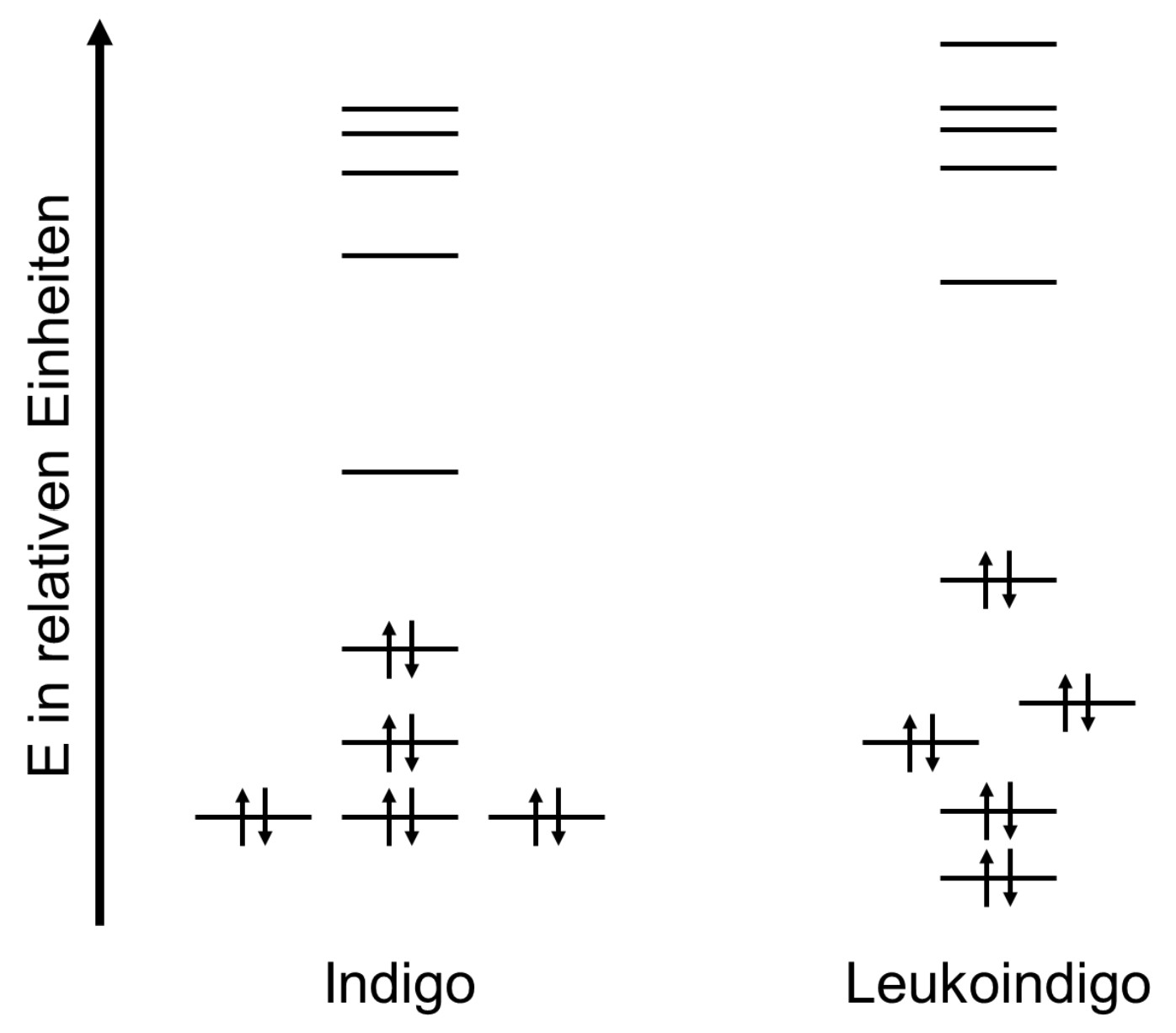
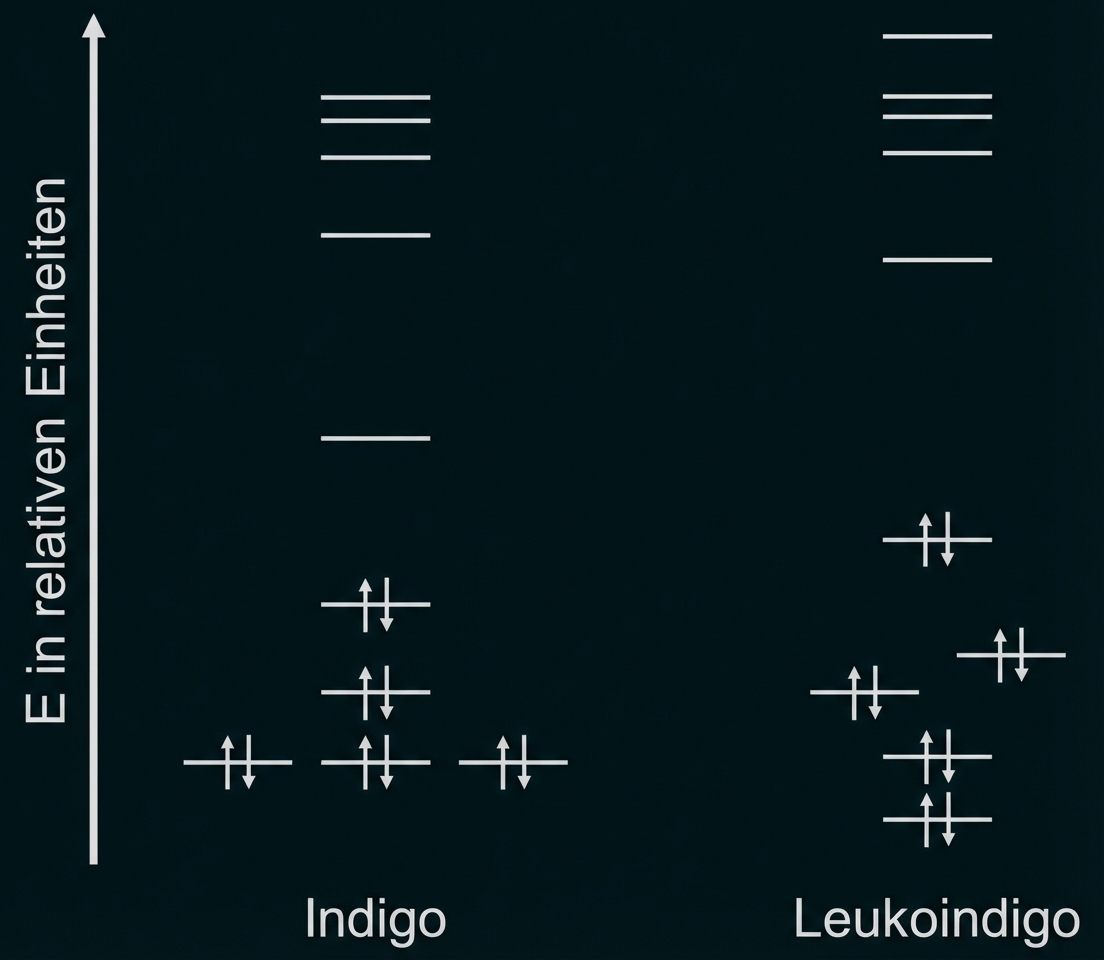
Abb. 4: Ausschnitte aus den MO-Schemata von Indigo und Leukoindigo2,3
Material 2: Säurerot
Bei Säurerot handelt es sich um eine Klasse von Farbstoffen, die bei niedrigen pH-Werten auf Fasern aufgetragen werden. So lassen sich mit z. B. Säurerot 73, einem Vertreter dieser Farbstoffklasse, u. a. Wolle, Seide oder Polyamidfasern färben.
Tab. 1: GHS-Gefahrstoffkennzeichnung von Säurerot 73
 
|
Signalwort: Achtung |
|
H315: Verursacht Hautreizungen. H319: Verursacht schwere Augenreizung. H335: Kann die Atemwege reizen. |
|
In einer Versuchsreihe wird bestimmt, welche Mengen an Säurerot 73 durch verschiedene Verfahren aus Färbereiabwässern entfernt werden können. Dazu wird zuerst eine fotometrische Eichreihe angelegt, die im Anschluss dazu verwendet wird, die Konzentrationen an Säurerot 73 bei den einzelnen Verfahren zu messen. Im eingesetzten Fotometer wurden Küvetten mit einer Schichtdicke der Lösung von verwendet.
Tab. 2: Messergebnisse für eine fotometrische Eichreihe mit Säurerot 73
|
Konzentration von Säurerot in mg/L |
Konzentration von Säurerot in µmol/L |
Extinktion |
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
|
Zur Entfernung von Säurerot 73 aus Färbereiabwässern stehen zwei Verfahren zur Verfügung:
1) Nanofiltration:
Hierbei wird Abwasser durch eine spiralförmig gewundene Membran mit sehr feinen Poren gepresst. Wasser-Moleküle können im Gegensatz zu Farbstoff-Molekülen die Membran passieren. Je weiter die Lösung durch die Spirale strömt, desto weniger Lösungsmittel ist in ihrem Inneren vorhanden, wodurch die Konzentration der gelösten Stoffe ansteigt (Abb. 5).
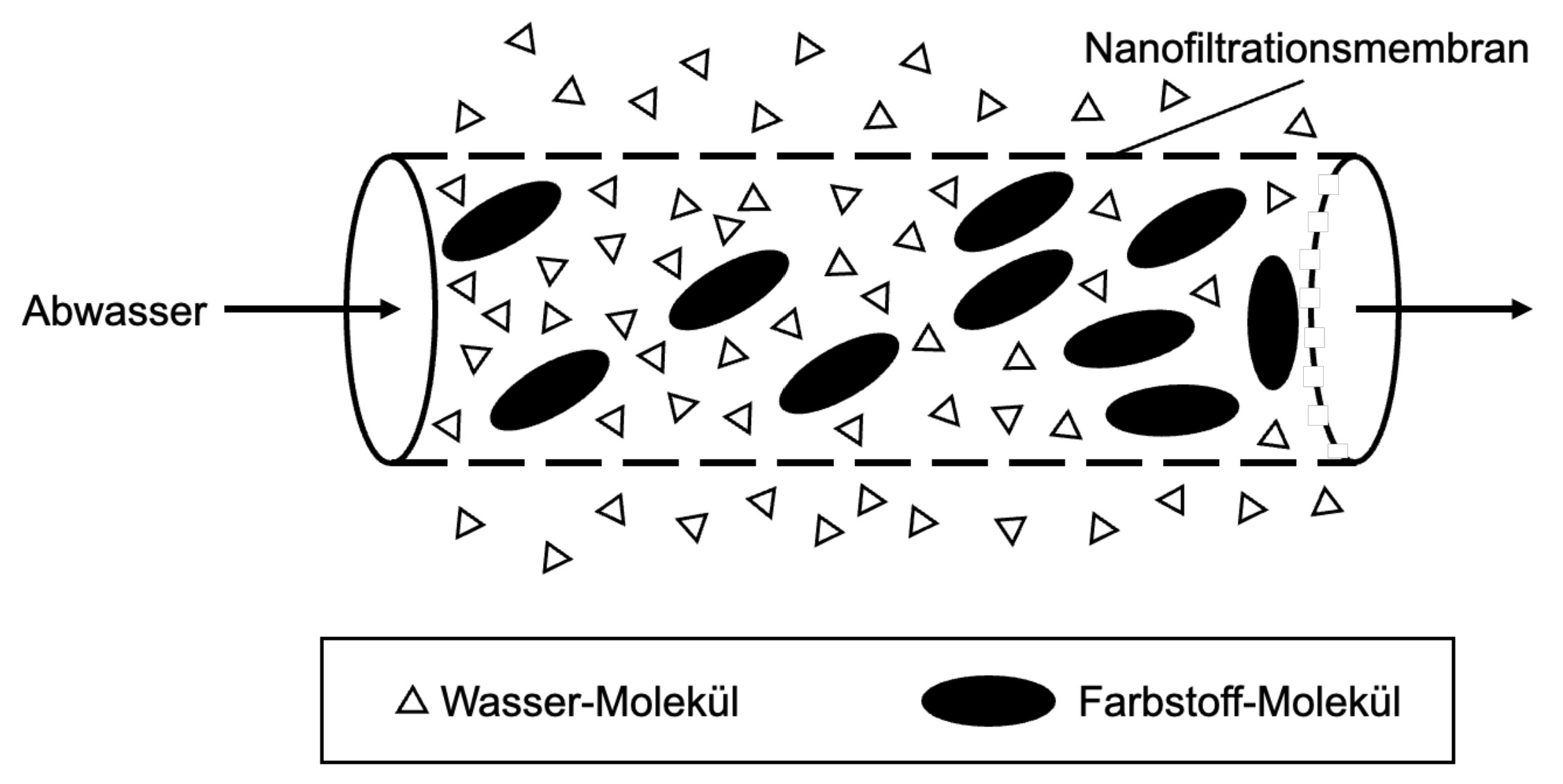
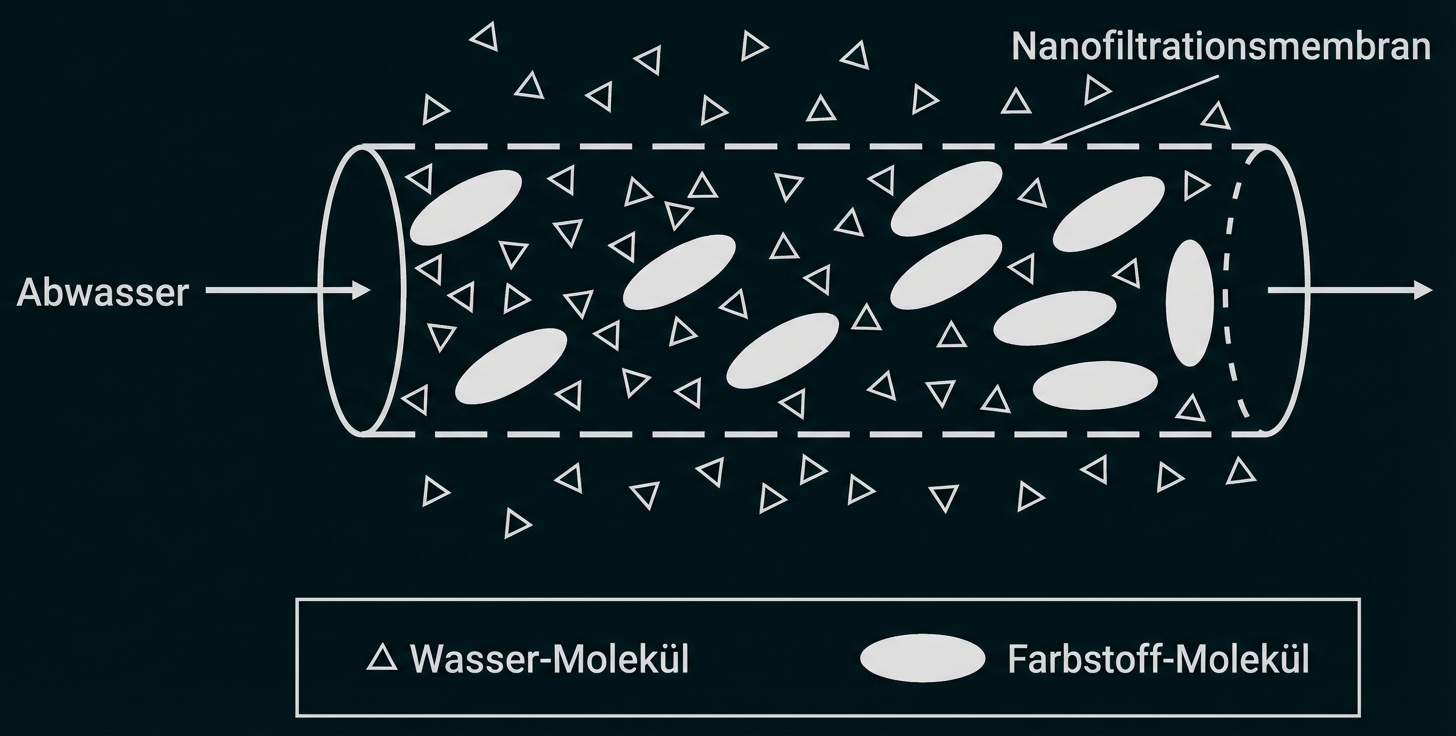
Abb. 5: schematische Darstellung der Nanofiltration5
Die Nanofiltrationsmembran hat eine Haltbarkeit von mehreren Jahren und besteht aus mehreren Schichten. Enthaltene Kunststoffe werden meist auf Erdölbasis hergestellt. Zwei Beispiele sind in den Abbildungen 6 und 7 dargestellt:
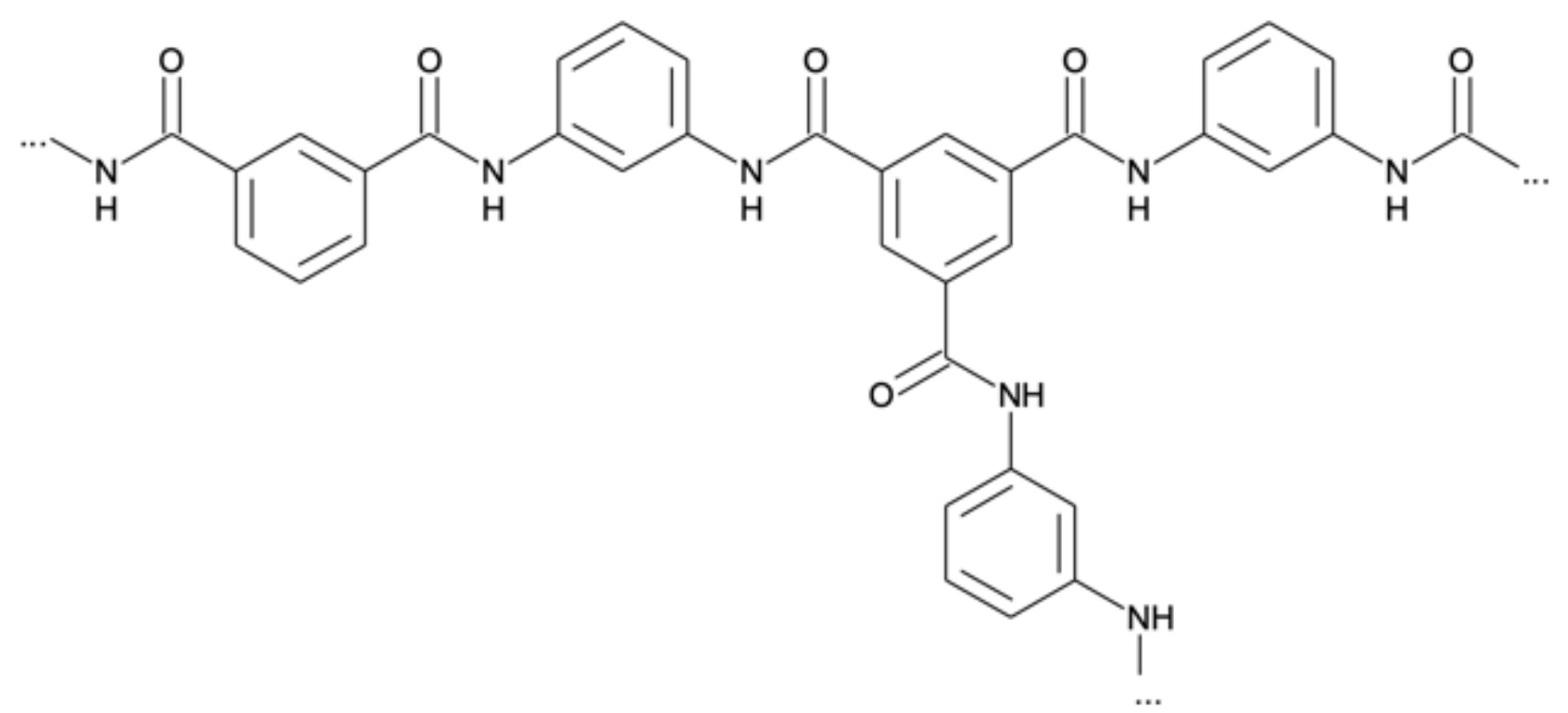
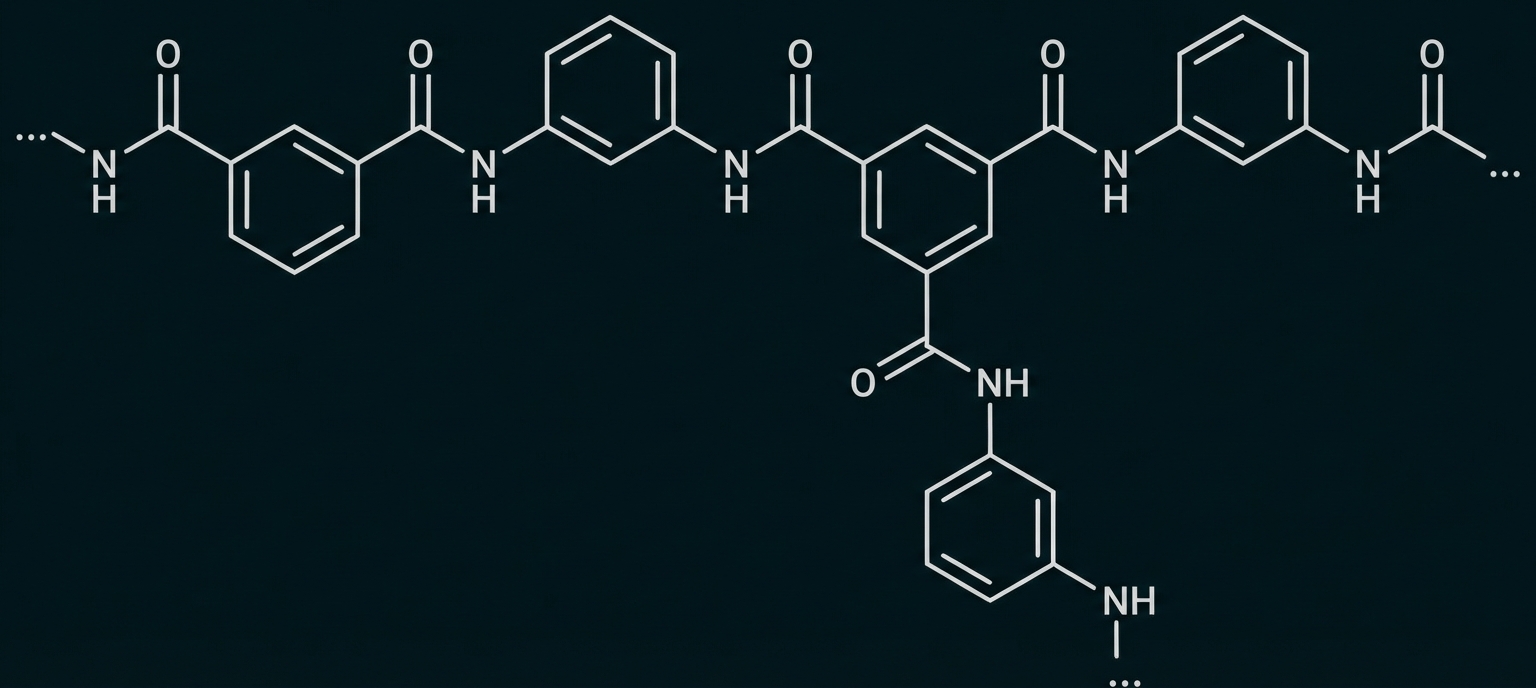
Abb. 6: Ausschnitt aus einem Aramid-Molekül
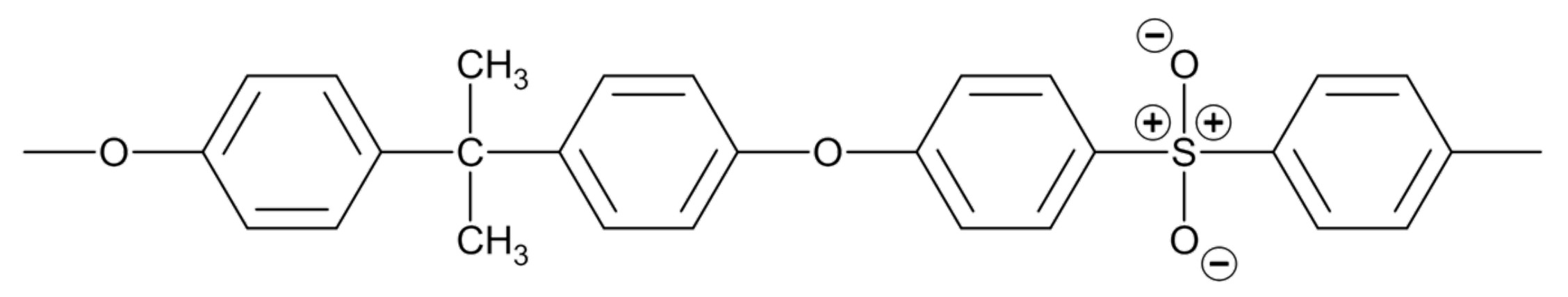
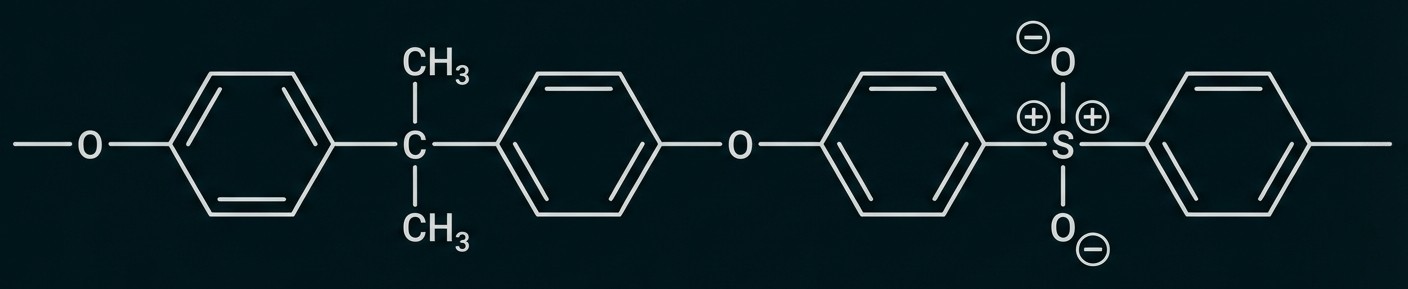
Abb. 7: Ausschnitt aus einem Polysulfon-Molekül
Der entfernte Farbstoffanteil bei Anwendung dieses Verfahrens ist in Abbildung 8 dargestellt.
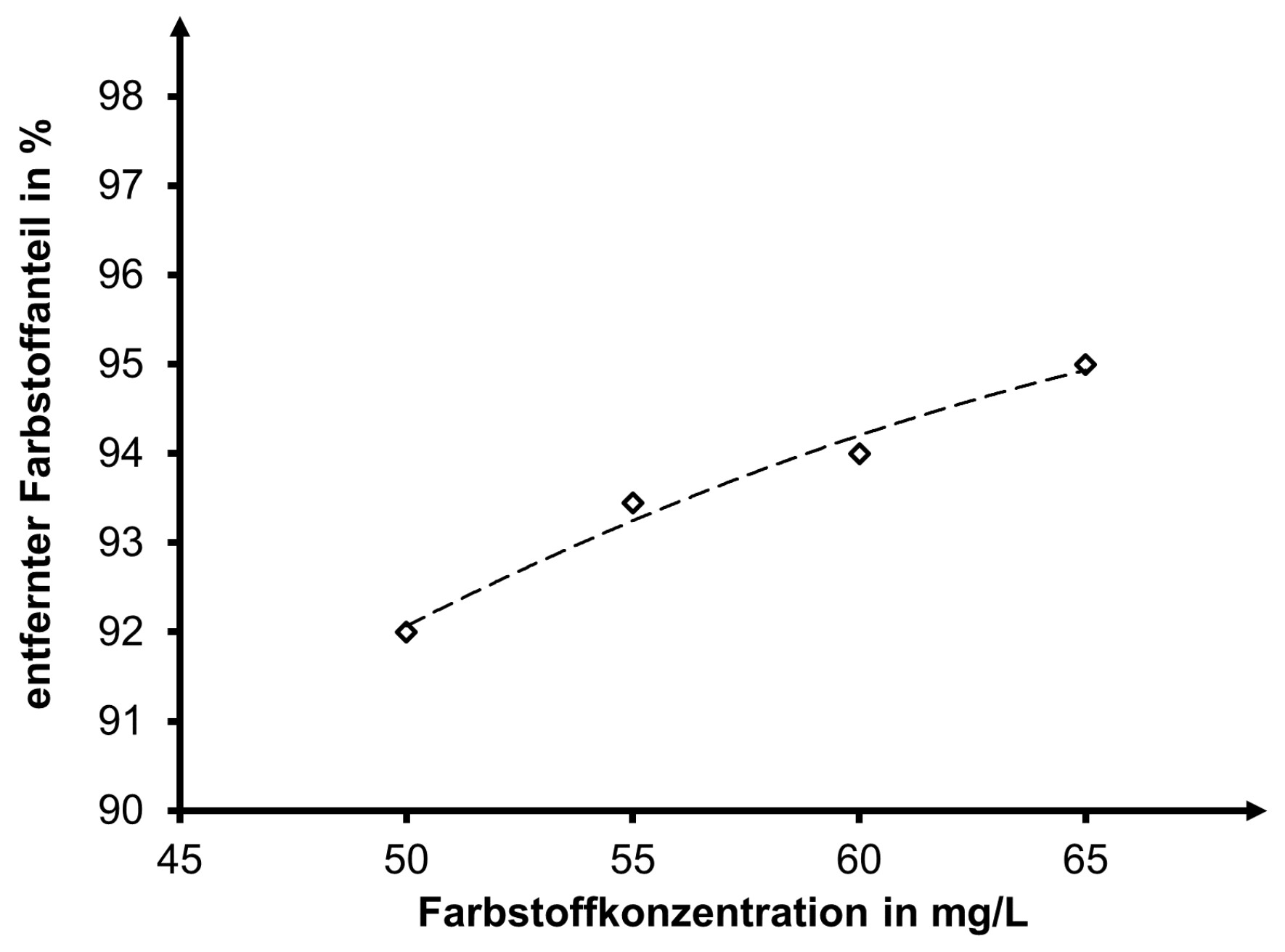
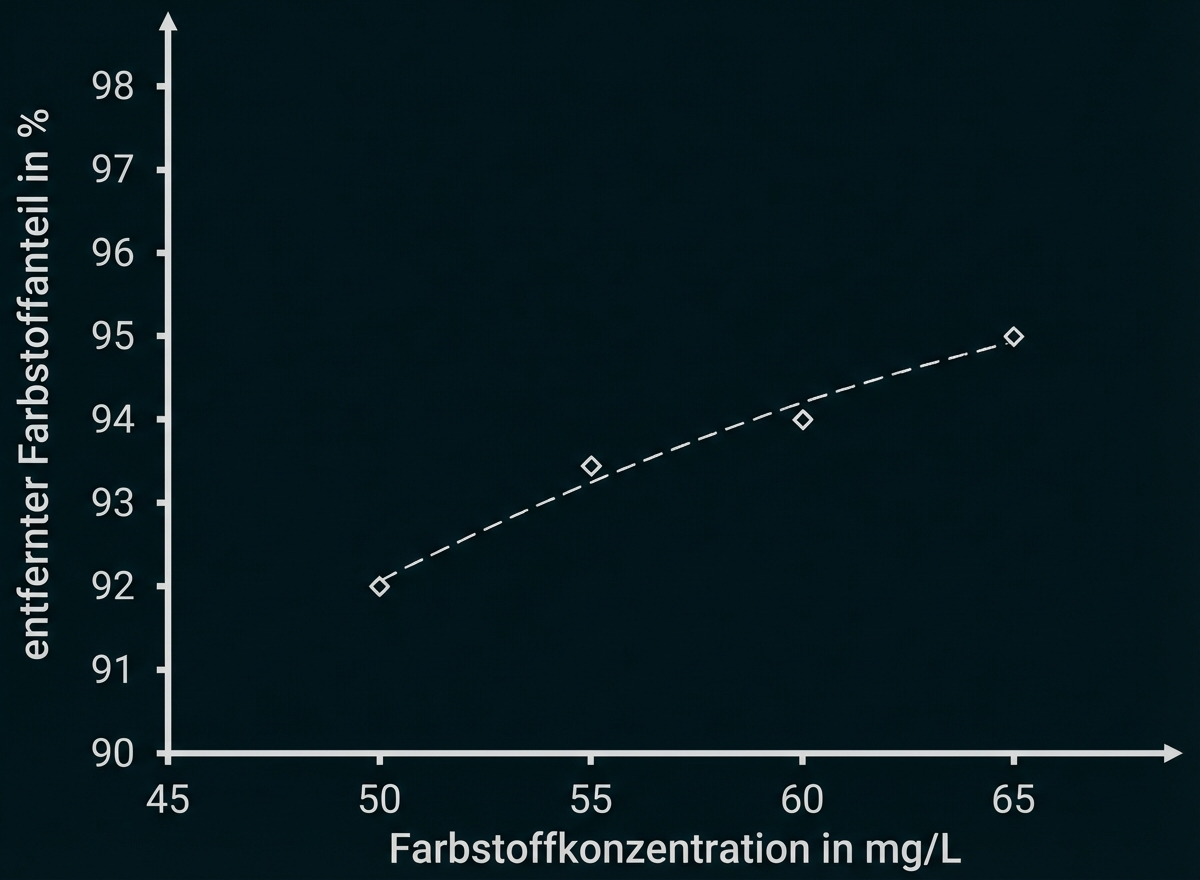
Abb. 8: durch Nanofiltration an einer Membran entfernter Farbstoffanteil von Säurerot 734
2) Adsorption:
Das Abwasser wird z. B. durch organisches Material wie den als Abfallprodukt bei der Herstellung von Reiswein anfallenden Bodensatz geleitet. Dabei lagert sich der Farbstoff an die Oberfläche des Adsorptionsmittels an und wird so gebunden. Abhängig von verschiedenen Faktoren können so pro Gramm Adsorptionsmittel ca. Farbstoff gebunden werden. Das Material mit dem gebundenen Farbstoff muss anschließend entsorgt werden. Abbildung 9 zeigt den durch Adsorption entfernten Anteil an Säurerot 73.
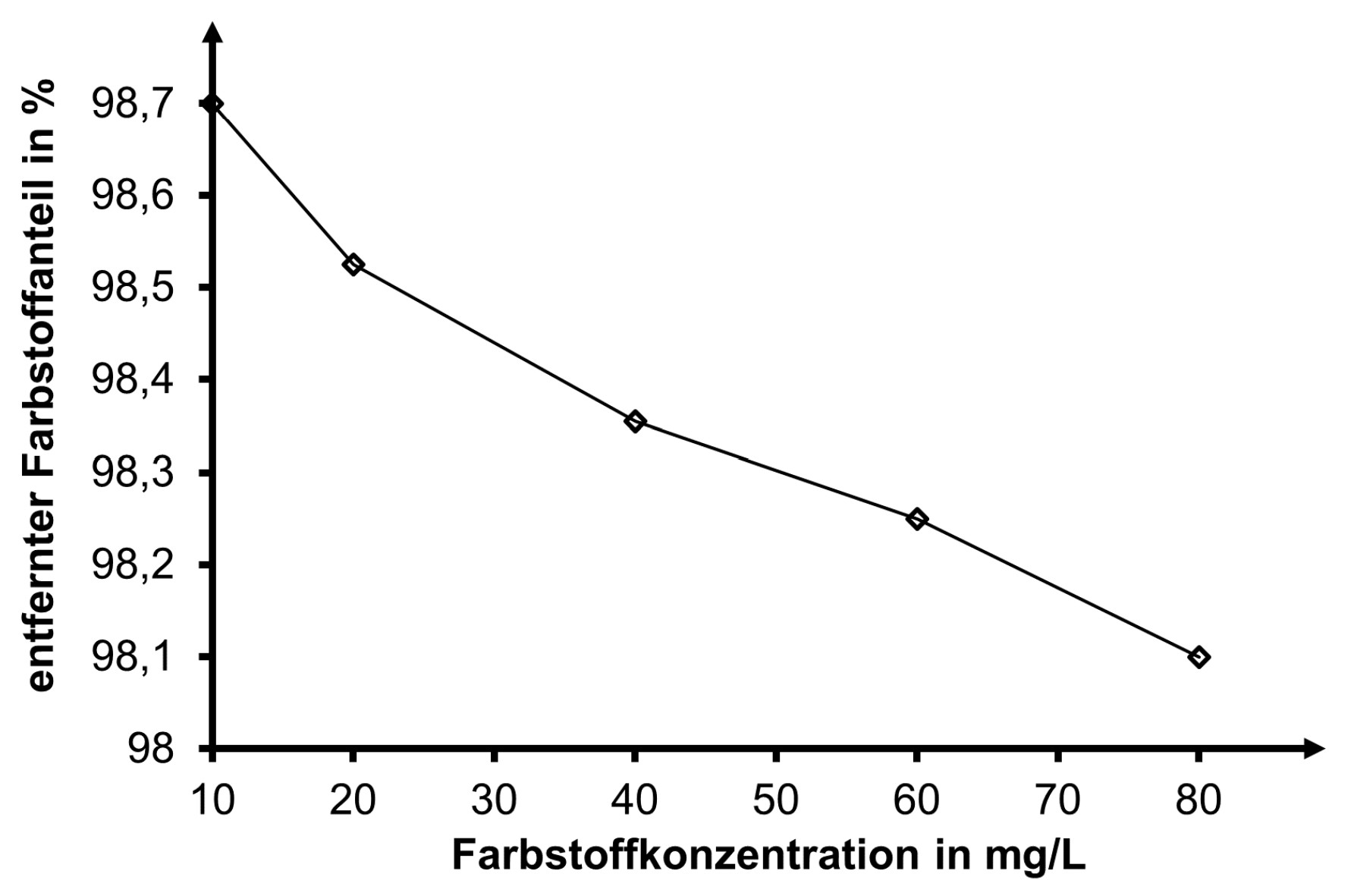
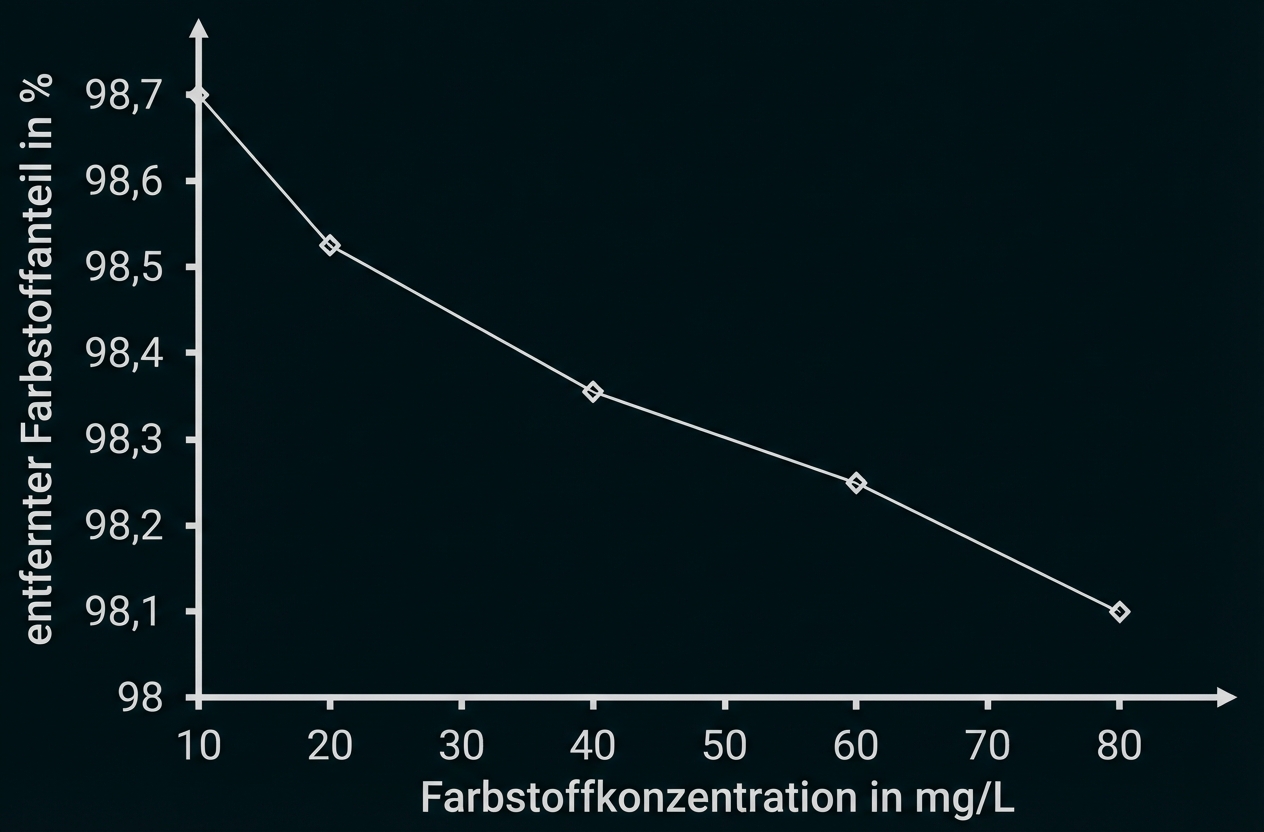
Abb. 9: durch Adsorption an den Bodensatz aus der Reisweinproduktion entfernter Farbstoffanteil von Säurerot 735
Quellen:
1 De Melo, J. S. S., Moura, A. a. P., & Melo, M. J. (2004). Photophysical and spectroscopic studies of indigo derivatives in their keto and leuco forms. Journal of Physical Chemistry A, 108(34), 6975–6981.
2 https://molvis.cup.uni-muenchen.de/site/assets/files/1048/leuko-indigoshmo.pdf
3 https://molvis.cup.uni-muenchen.de/site/assets/files/1048/indigoshmo.pdf
4 Abid, M. F., Zablouk, M. A., & Abid-Alameer, A. M. (2012). Experimental study of dye removal from industrial wastewater by membrane technologies of reverse osmosis and nanofiltration. Iranian Journal of Environmental Health Science & Engineering, 9(1).
5 Wang, Q., Liang, L., Xi, F., Tian, G., Mao, Q., & Meng, X. (2020). Adsorption of Azo Dye Acid Red 73 onto Rice Wine Lees: Adsorption Kinetics and Isotherms. Advances in Materials Science and Engineering, 2020, 1–8.
Weiter lernen mit SchulLV-PLUS!
monatlich kündbarSchulLV-PLUS-Vorteile im ÜberblickDu hast bereits einen Account?Leukoindigo ist aufgrund der Ladungen im Molekül im Gegensatz zu Indigo wasserlöslich. Die Kleidungsfasern werden in die wässrige Leukoindigo-Lösung getaucht, womit die Leukoindigo-Moleküle in die Fasern gelangen. Im Anschluss lässt man die nassen Fasern an der Luft trocknen, wodurch das Leukoindigo in der Rückreaktion wieder zu Indigo oxidiert wird.
Hinreaktion: Reduktion von Indigo zu Leukoindigo
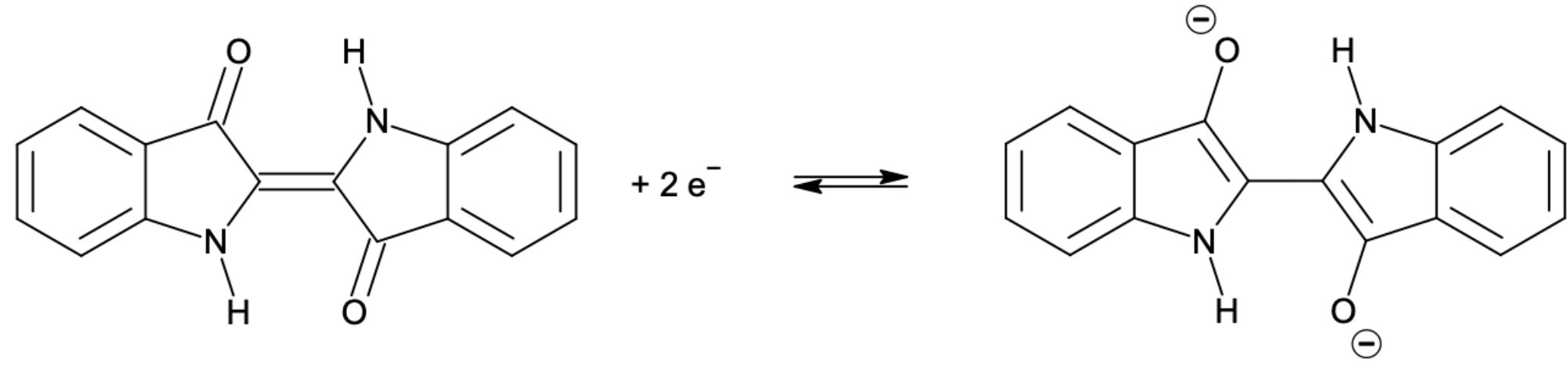

Als Reduktionsmittel kommt Dithionit zum Einsatz, das nach folgender Reaktionsgleichung oxidiert wird:
Rückreaktion: Das Oxidationsmittel ist hierbei Sauerstoff:
Das so direkt in der Faser hergestellte Indigo ist wasserunlöslich, lässt sich damit nicht mehr auswaschen und ist durch die Einbettung in der Faser teilweise vor mechanischem Abrieb geschützt.
Die Absorptionsmaxima liegen für Indigo bei ca. und für Leukoindigo bei ca.
Die Absorption bei Wellenlängen von weniger als
liegt im UV-Bereich und hat damit keinen Einfluss auf die Farbe.
Indigo absorbiert damit orange-rotes Licht am stärksten und erscheint damit in der Komplementärfarbe Blau.
Leukoindigo absorbiert am stärksten violett-blaues Licht und erscheint damit gelb-orange.
Die Energiedifferenz zwischen HOMO und LUMO ist beim Leukoindigo-Molekül deutlich größer als beim Indigo-Molekül, weshalb mehr Energie zur Anregung der Elektronen nötig ist. Die Wellenlänge des absorbierten Lichts bei Leukoindigo ist damit kleiner. Die MO-Schemata und das Absorptionsspektrum decken sich.
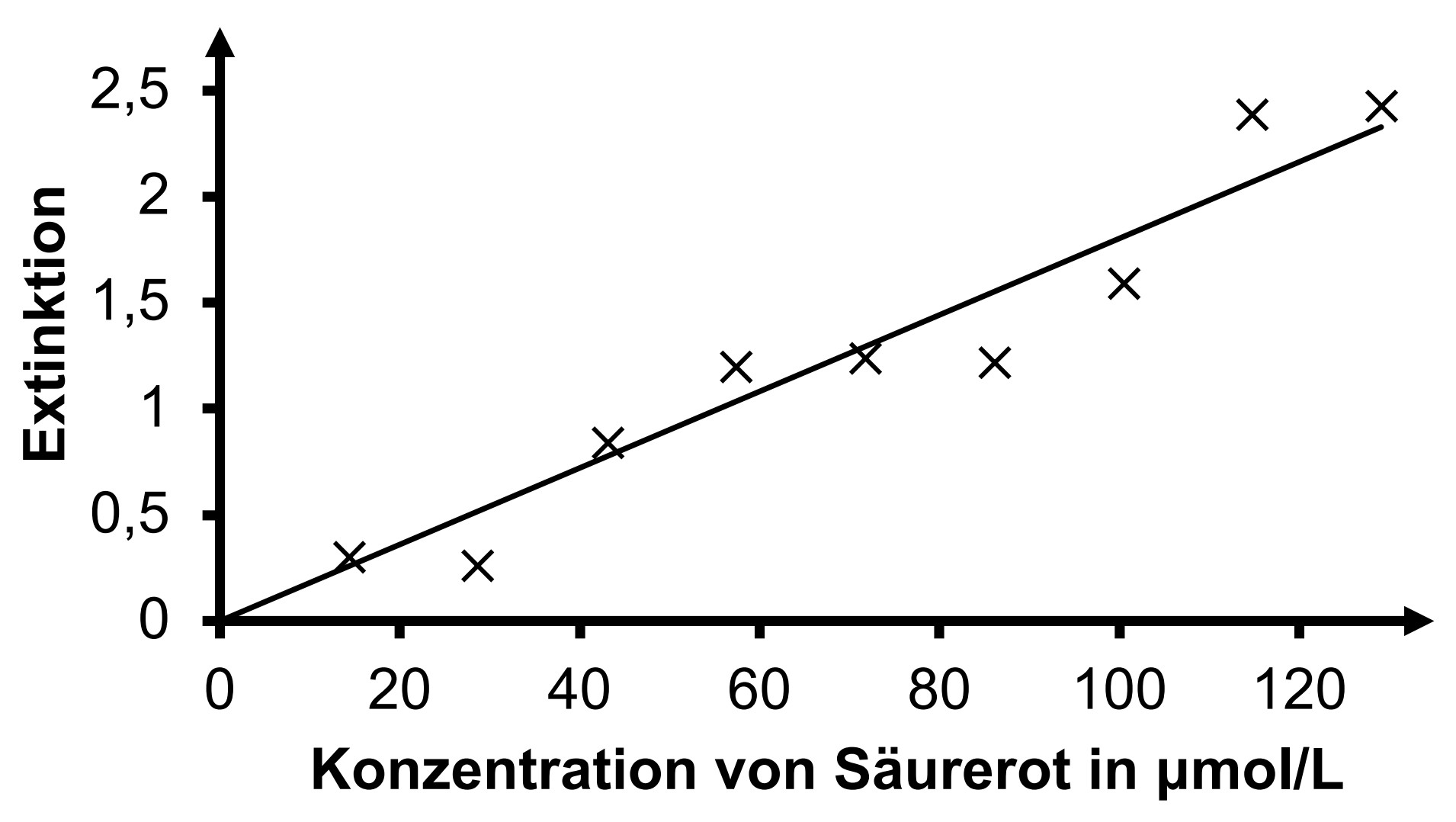
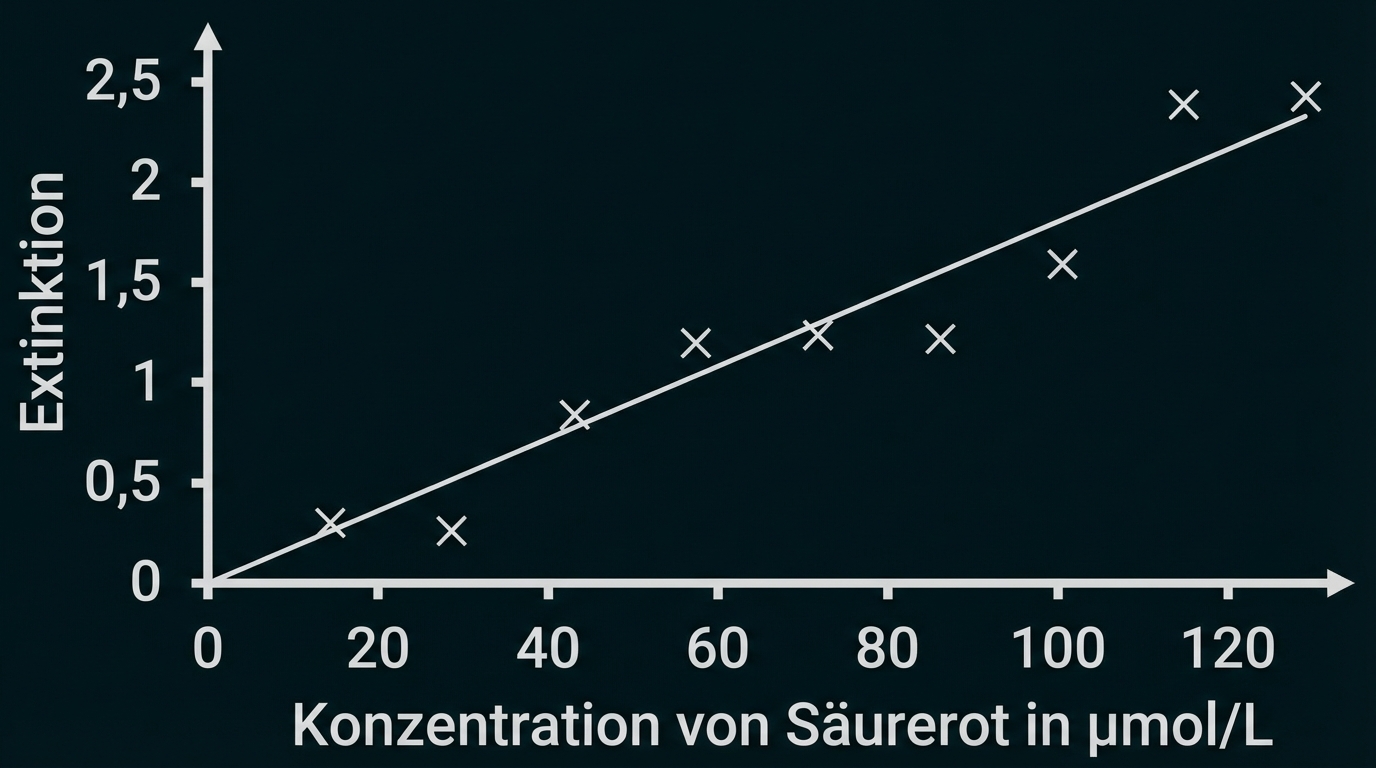
Bestimmung der Steigung der Geraden:
Somit:
Mit dem Lambert-Beerschen Gesetz gilt:
Das Aramid-Molekül weist Amidgruppen auf und wurde über eine Polykondensation hergestellt.
Für den linearen Molekülteil benötigt man als Monomere 1,3-Diaminobenzol und Benzol-1,3-dicarbonsäure, für die Verzweigungen muss zusätzlich Benzol-1,3,5-tricarbonsäure zugesetzt werden.
Beim Aramid treten regelmäßige Verzweigungen auf, wodurch eine dreidimensional vernetzte Struktur vorliegt, beim Polysulfon handelt es sich ausschließlich um lineare Moleküle.
Das Aramid ist ein Duroplast, damit eher hart und schmilzt beim Erwärmen nicht, bevor es sich zersetzt. Das Polysulfon ist ein Thermoplast ist und wird beim Erhitzen erst weich und schmilzt anschließend, bevor es sich zersetzt.
Die Kunststoffmembranen bei der Nanofiltration werden aus fossilen Rohstoffen hergestellt und sind demnach nicht besonders nachhaltig. Die Haltbarkeit der Membran ist relativ hoch und sie muss lange nicht ausgetauscht werden. Es fällt eine Lösung mit relativ hoher Konzentration an Schadstoffen an, womit die Abfallmenge eher niedrig ist.
Der Bodensatz aus der Reisweinproduktion ist ein nachwachsender Rohstoff. Er muss aufgrund der begrenzten Adsorptionsfähigkeit in relativ kurzen Abständen ausgetauscht werden und wird daher in großen Mengen benötigt. Die Menge an Abfällen nimmt bei der Adsorption stark zu, weil nicht nur der Farbstoff, sondern auch das verwendete Adsorptionsmittel mit entsorgt werden muss. Durch Adsorption können im Vergleich zur Filtration etwas höhere Anteile der Farbstoffe aus dem Abwasser entfernt werden.
Die ungefilterte Einleitung in Gewässer benötigt eigentlich keine Ressourcen und Abfälle werden direkt entsorgt, führt aber zu Umwelt-, Natur- und Gesundheitsschäden.
Abschließendes Urteil:
Z. B.: Eine ungefilterte Einleitung der Abwässer ist aufgrund der zu erwartenden Umwelt-, Natur und Gesundheitsschäden (vgl. GHS-Kennzeichnung) nicht zu vertreten, weshalb eines der beiden Verfahren zur Entfernung eingesetzt werden sollte.
Von den beiden Verfahren zur Entfernung des Farbstoffs ist die Nanofiltration als überlegen anzusehen, da diese in der Farbstoffentfernung zwar weniger effizient ist, aber aufgrund der langen Haltbarkeit der Membran im Langzeitbetrieb wahrscheinlich nachhaltiger ist, als die Adsorption mittels Pflanzenmaterial.